Formaliser une évaluation des risques pour les excipients
Les excipients jouent un rôle essentiel dans la production des formes posologiques finales des médicaments et des produits biologiques. Ils facilitent le processus de fabrication (par exemple, les agents anti-agglomération) et protègent, soutiennent et améliorent la stabilité. Ils peuvent également améliorer la biodisponibilité. De plus, les excipients aident à maintenir la sécurité ou la fonction du produit pendant son stockage et son utilisation.
N’étant plus considérés comme des accompagnements inertes d’un principe actif, les excipients sont l’objectif d’une intensification de la pression en faveur d’une gestion de la qualité plus rigoureuse, imposant de nouvelles exigences à la fois aux fournisseurs et aux utilisateurs. Réguler la qualité des excipients n’est cependant pas une mince tâche. Le marché mondial devrait dépasser les 5 milliards de dollars d’ici 2020 – avec un taux de croissance de 6,0% de 2014 à 2020 (1). Des milliers d’excipients différents sont disponibles et seul un faible pourcentage d’entre eux est fabriqué uniquement à des fins pharmaceutiques.
Depuis de nombreuses années, les exigences en matière de BPF relatives aux IPA sont clairement définies, notamment le chapitre 2 des principes de l’UE, 21 CFR, partie 11 et le document ICH Q7: Bonnes pratiques de fabrication pour les ingrédients pharmaceutiques actifs. Mais, jusqu’à récemment, les exigences BPF bien définies et strictes applicables aux excipients n’existaient pas.
Un accent sur la qualité
L’industrie pharmaceutique utilise de plus en plus les principes de gestion des risques pour mieux protéger les patients; Cette attention renouvelée à la sécurité inclut désormais les excipients. Dans le même temps, les autorités de régulation ont demandé des lignes d’approvisionnement plus sûres et des mesures de qualité clairement définies pour les excipients.
En 2011, la directive de l’Union européenne sur les médicaments falsifiés a établi que les titulaires d’autorisations de fabrication doivent utiliser une évaluation des risques formalisée afin de s’assurer du respect des BPF permettant de garantir l’adéquation de l’excipient (2). Dans le cadre de cette évaluation des risques, les fabricants doivent prendre en compte à la fois la source et l’utilisation prévue des excipients en question. La directive a ensuite indiqué que la Commission européenne envisageait d’adopter des lignes directrices pour l’adoption de BPF appropriées pour les excipients. Après de vives discussions, des lignes directrices concernant le processus de gestion des risques et une orientation sur le niveau approprié de BPF pour les excipients ont été publiées en mars 2015.
Ces lignes directrices s’appliquent non seulement aux médicaments fabriqués en Europe, mais également aux produits fabriqués hors d’Europe et destinés au marché européen. Les régulateurs attendent maintenant des importateurs qu’ils fournissent des évaluations des risques et des documents connexes.
À compter du 21 mars 2016, les utilisateurs des excipients et les fabricants de médicaments de l’UE étaient légalement tenus de mettre en œuvre les exigences relatives aux BPF, y compris les évaluations des risques complétées pour chaque excipient utilisé.
Gardez à l’esprit que, même si la réglementation concernant les BPF pour les IPA définit clairement ce qui est nécessaire pour la conformité, les directives d’évaluation des risques pour les excipients ne sont que cela – des directives qui offrent des outils et un cadre pour la détermination des BPF appropriées. Cela laisse l’entière responsabilité de définir les BPF applicables comme «nécessaires» aux excipients d’un produit pharmaceutique spécifique entre les mains du titulaire de l’autorisation de mise sur le marché.
D’autres pays développent également des exigences formelles pour les BPF des excipients. La FDA américaine évalue et autorise l’utilisation d’excipients dans le cadre d’une demande de nouveau médicament. En vertu de la législation américaine, un nouvel excipient pharmaceutique, contrairement à un médicament actif, n’a aucun statut réglementaire à moins d’être qualifié au moyen d’un ou plusieurs des mécanismes d’homologation disponibles pour les composants utilisés dans les formes galéniques finies.
En 2012, la loi sur la sécurité et l’innovation de la Food and Drug Administration (FDASIA) a été promulguée, renforçant l’autorité de l’Agence et renforçant sa capacité à protéger et à faire progresser la santé publique par le biais de nombreuses activités, notamment l’amélioration de la sécurité de la chaîne d’approvisionnement en médicaments. FDASIA comprend un ensemble de dispositions, contenues dans le titre VII de la loi, qui donne aux nouvelles autorités de la FDA le pouvoir de relever les défis posés par les chaînes d’approvisionnement en médicaments qui se mondialisent de plus en plus (3). L’une de ces nouvelles autorités exige que les fabricants incluent, dans le cadre d’une liste de médicaments, le nom, l’adresse et les identifiants d’installation uniques des fabricants d’excipients associés.
En 2013, la FDA a lancé le programme pilote de sécurisation de la chaîne logistique afin de renforcer les contrôles sur les importations de médicaments. L’objectif était de concentrer les ressources de surveillance des importations de l’Agence sur la prévention de l’entrée de médicaments à haut risque susceptibles de compromettre la qualité et la sécurité de l’approvisionnement en médicaments des États-Unis. Le programme pilote, qui s’est achevé en février 2016, a permis à la FDA d’évaluer son efficacité pour améliorer la conformité des médicaments importés avec les réglementations de la FDA et la sécurité de la chaîne d’approvisionnement en médicaments.
Mise en œuvre de l’évaluation des risques
ICH Q9: Quality Risk Management offre des conseils pour l’évaluation des risques selon deux principes:
- La description des risques devrait reposer sur des connaissances scientifiques et devrait être liée à la protection du patient.
- Le niveau d’effort, de formalité et de documentation du processus de gestion des risques qualité (QRM) doit être en rapport avec le niveau de risque présenté par l’excipient.
Le risque d’excipient est évalué sur la base des dommages causés par des dangers microbiologiques, chimiques (toxicologiques, pathologiques) ou physiques (étouffement, irritation). Le risque varie en fonction de la voie d’administration du produit pharmaceutique (orale, inhalée, injectée) et de la fonction de l’excipient. Un excipient utilisé comme charge, par exemple un liant ou un colorant, pourrait présenter un risque plus faible que celui utilisé comme stabilisant ou comme véhicule pour une libération contrôlée, ce dernier pouvant affecter la biodisponibilité. Cependant, les exigences BPF et les stratégies de contrôle d’un excipient utilisé comme charge dans une application orale seraient complètement différentes de celles utilisées pour la libération contrôlée d’une substance médicamenteuse dans un produit biologique.
Un certain nombre d’approches pour l’évaluation des risques de qualité et des conseils sont disponibles. La figure 1 présente un modèle d’évaluation des risques développé par le Conseil international des excipients pharmaceutiques (IPEC Europe) et le groupe Qualité pharmaceutique (PQG), avec le soutien de la Fédération européenne des industries et associations pharmaceutiques (EFPIA). Le modèle combine l’approche de l’ICH Q9 avec les exigences spécifiques de la directive de l’UE sur l’évaluation des risques et met en évidence la nécessité pour l’utilisateur excipient et le fabricant de collaborer étroitement au processus d’évaluation. Un fabricant d’excipients effectuant une évaluation des risques similaire devrait travailler en étroite collaboration avec l’utilisateur pour comprendre la fonction que l’excipient est censé remplir, ainsi que la voie d’administration.
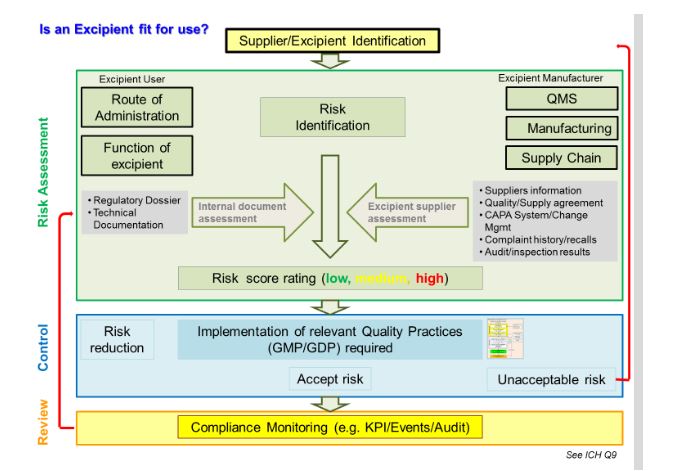
Figure 1 Processus d’évaluation des risques liés aux excipients
* P. Rafidison, F. Holtz, S. Rönninger, Une approche pratique de la mise en œuvre des BPF pour les excipients, Pharm. Tech., Septembre 2014, 26-36 (4)
Définir les BPF appropriées
La bonne nouvelle est que les fabricants et les utilisateurs d’excipients n’ont pas besoin de développer leurs propres BPF. Un certain nombre de normes de l’industrie bien établies, acceptées et volontaires existent et peuvent être suivies. Ceux-ci inclus:
- IPEC-PQG Guide GMP, 2006
- Chapitre général USP <1078>
- EXCiPACT MC
- NSF / IPEC / ANSI-363-2014
Dans de nombreux cas, l’application de ces normes sera probablement suffisante pour la plupart des excipients.Mais un petit nombre d’excipients pourrait présenter des risques pour les patients. Celles-ci peuvent nécessiter l’application de contrôles plus approfondis que ceux recommandés dans les normes volontaires. Par exemple, un excipient utilisé dans une administration parentérale pourrait être soumis à des directives sur la fabrication de médicaments stériles, comme prévu dans le volume 4 d’EudraLex, le régime régissant les médicaments dans l’Union européenne (5).
Une perspective positive
Une meilleure compréhension du rôle que jouent les excipients dans l’innocuité et les performances cliniques des médicaments a attiré l’attention sur le risque qu’ils peuvent également présenter pour les patients, ce qui définit la nécessité de disposer de bonnes BPF pour les excipients. Une attention accrue portée aux chaînes d’approvisionnement et une communication plus solide entre les fournisseurs d’excipients et les fabricants de médicaments sont essentielles pour garantir la sécurité des patients. Les fabricants de médicaments doivent s’attendre à ce que leurs fournisseurs fournissent des dossiers accompagnant chaque excipient avec des informations appuyant l’évaluation des risques du fabricant. Il peut s’agir de données sur la fabrication, les tests, la chaîne d’approvisionnement et le système qualité appliqué, ou d’informations montrant l’alignement sur les directives réglementaires.
Les principes d’évaluation des risques et de gestion des risques qualité largement utilisés dans les industries pharmaceutique et biotechnologique sont en cours d’adoption pour les excipients. La directive européenne sur l’évaluation des risques est celle que les fournisseurs et les utilisateurs peuvent appliquer afin de déterminer le niveau approprié de BPF, d’accroître l’assurance de l’intégrité de la chaîne d’approvisionnement et de mieux protéger les patients.
Références
- « Analyse du marché des excipients selon les polymères (MCC, HPMC, CMC, Ethylcellulose, Povidone), les alcools (Glycérine, Sorbitol, Mannitol, Propylène Glycol), les minéraux (Argile, Dioxyde de silicium, Dioxyde de titane), les sucres et les segments jusqu’à 2020. » Recherche Grand View. Septembre 2015.
- «Directive 2011/62 / EU.» Journal officiel de l’Union européenne 54 (2011): 74-87.
- «FDASIA Title VII Overview.». US Food and Drug Administration. 15 septembre 2015.
- Rafidison, P., Holtz, F. et Rönninger, S. «Une approche pratique de la mise en œuvre des BPF pour les excipients», Pharmaceutical Technology 38 (2014): 26–36.
- “Annexe 1: Principes directeurs de l’UE en matière de bonnes pratiques de fabrication des médicaments à usage humain et à usage vétérinaire.” Commission européenne. 25 novembre 2008.
* Remerciements spéciaux à Patricia Rafidison, Dow Corning et Stephan Rönninger, Amgen (Europe) GmbH

 Biologiste, Frithjof Holtz a travaillé pendant 25 ans pour le secteur des sciences de la vie de Merck KGaA, à Darmstadt, en Allemagne, dont plus de dix ans dans les domaines de l’assurance qualité et de la réglementation.
Biologiste, Frithjof Holtz a travaillé pendant 25 ans pour le secteur des sciences de la vie de Merck KGaA, à Darmstadt, en Allemagne, dont plus de dix ans dans les domaines de l’assurance qualité et de la réglementation.











