Levothyrox : «Je n’avais jamais connu une telle crise sanitaire»
13 octobre 2017

Gérard Bapt, médecin et ancien député, estime que les autorités n’ont pas pris la mesure de la crise à laquelle sont confrontés les patients traités avec le Levothyrox.
Ancien député (PS) de Haute- Garonne spécialiste des questions de santé, le médecin Gérard Bapt est connu pour avoir été le premier politique à soulever l’affaire du Mediator (un antidiabétique pris comme coupe-faim et soupçonné d’avoir provoqué des centaines de décès).
Que vous évoquent des sites Internet proposant du Levothyrox à plus de 100 € ?
Gérard Bapt. De vives inquiétudes. J’avais dès le 2 septembre alerté le ministère sur les manoeuvres frauduleuses qui se développent sur Internet. Le risque est que des patients prennent des médicaments contrefaits avec des conséquences très graves sur leur santé. Mais si ce type de sites existe, c’est aussi parce que les autorités n’ont pas pris la mesure de la crise et ont fait preuve de contradictions, inquiétant les patients. Même si des lots de l’ancienne formule ont finalement été réintroduits en France, certains ont tellement peur de ne pas y avoir accès qu’ils sont prêts à tout pour s’en procurer.
Mercredi, l’Agence du médicament a indiqué avoir reçu 14 633 signalements d’effets indésirables, soit 0,6 % des patients traités…
Ce rapport d’étape minimise les faits. Il oublie les milliers de dossiers en attente de traitement dans les centres de pharmacovigilance, débordés ! La crise est loin d’être terminée.
LIRE AUSSI
>Les clés pour comprendre le scandale Levothyrox
Comment en êtes-vous si sûr ?
Hier encore, j’étais au téléphone avec un psychiatre qui m’indiquait avoir eu plusieurs hospitalisations à cause de troubles liés à la nouvelle formule du Levothyrox. Nous sommes sollicités de toute part. Je n’avais jamais connu une telle crise sanitaire.
Même avec le Mediator, dont vous avez porté le dossier ?
Quand j’ai organisé dans ma commune (NDLR : Saint-Jean, Haute-Garonne) la première réunion Mediator avec Irène Frachon, il y avait 200 personnes. Pour celle sur la Dépakine, il y avait 120 personnes. Dimanche, j’ai organisé celle sur le Levothyrox, Nous avions prévenu à peine cinq jours avant et il y avait 900 personnes, pas assez de places assises. Le Levothyrox dépasse tout en termes d’impact sur la population comme de mobilisation. Il faut une vraie réflexion sur les solutions à mettre en oeuvre et en finir définitivement avec le monopole de Merck sur ce médicament.
Le Parisien
LEVOTHYROX : premiers résultats de l’enquête de pharmacovigilance de l’ANSM, des zones d’ombre persistent
Par Jean-philippe RIVIERE
Date de publication : 12 Octobre 2017
L’ANSM a effectué une analyse intermédiaire des signalements d’effets indésirables effectués entre fin mars (mise en vente de la nouvelle formulation de LEVOTHYROX) et mi-septembre 2017.
Les résultats, présentés au comité technique de pharmacovigilance, montrent un nombre de signalement d’effets indésirables inédit depuis la mise en circulation de la nouvelle formulation de LEVOTHYROX : 14 633 signalements reçus par les centres régionaux de pharmacovigilance en 6 mois, ce qui représente 0,59 % des patients traités avec cette nouvelle formule.
Cette première analyse porte sur 5 062 cas, les plus documentés, sur ces 14 633.
En moyenne, 5 effets indésirables ont été signalés par patient.
Les événements les plus fréquemment rapportés sont une fatigue, des maux de tête, insomnies, vertiges, douleurs articulaires ou musculaire, ou encore une perte de cheveux.
Ils étaient déjà rapportés avec ce médicament, mais à une fréquence moindre. Cette enquête n’a par contre pas mis en évidence de nouveaux effets indésirables.
Lorsque la TSH était documentée, des déséquilibres ont été constatés dans plus d’un tiers des cas. L’ajustement des doses ne semble pas produire de résultat, mais le recul est insuffisant. Par contre, le retour à l’ancienne formule semble efficace.
Les auteurs notent que même en l’absence de déséquilibre thyroïdien, des symptômes non spécifiques ont été notifiés, ce qui, selon les auteurs, interpelle et « mérite plus d’investigations » pour rechercher d' »autres facteurs ».
Les premiers résultats de l’enquête de pharmacovigilance de l’ANSM montrent une forte hausse des signamenets d’effets indésirables en juillet et en août (section d’un graphe reproduit ci-dessous).
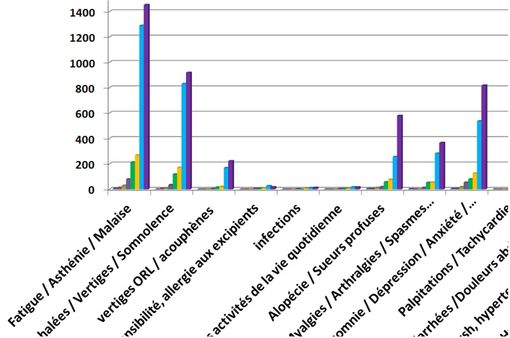
Une enquête de pharmacovigilance débutée dès mars 2017, en raison du constat antérieur de déséquilibres lors de changements de formule
L’expérience de la substitution de LEVOTHYROX par les génériques en 2011 ayant montré un risque de déséquilibre thyroïdien en cas de changement de formulation, une equête de pharmacovigilance a été initiée en mars 2017 par l’ANSM dès le début de la mise en circulation de la nouvelle formulationde LEVOTHYROX (lévothyroxine).
Cette enquête a donc été mise en place pour surveiller le profil de sécurité de LEVOTHYROX dans le contexte de changement de formule, notamment les potentielles perturbations de l’équilibre thyroïdien et le risque d’erreurs médicamenteuses.
Pour rappel, LEVOTHYROX nouvelle formule contient du mannitol et de l’acide citrique en remplacement du lactose, ceci afin d’améliorer la stabilité de la teneur en levothyroxine (voir notre article de mars 2017).
Une enquête élargie à l’analyse de l’ensemble des effets indésirables signalés
L’objectif initial de cette étude a été élargi à l’analyse de l’ensemble des effets indésirables rapportés en raison de l’augmentation importante des signalements à partir deu mois d’août (voir notre article du 23 août).
Les premiers résultats de cette enquête ont été présentés au CTPV (comité technique de pharmacovigilance) le 10 octobre.
Analyse d’environ 9 000 cas (sur 14 633 personnes signalant des effets indésirables), soit 0,59 % des personnes sous LEVOTHYROX
L’analyse porte sur les données issues :
- des bases de données du laboratoire Merck recueillies entre le 27 mars et le 10 septembre : 3 890 cas ont été rapportés avec la nouvelle formule (4 478 cas au total) , dont 13 % avec un critère de gravité ;
- de la base nationale de pharmacovigilance (BNPV) entre le 27 mars et le 15 septembre : 5 062 cas y ont été enregistrés, parmi les 14 633 signalements effectués sur le portail du ministère (représentant 0,59 % des 2,6 millions de patients traités par la nouvelle formule de LEVOTHYROX, source : Assurance maladie). Ces 5 062 cas (dont 1 150 évocateurs d’une dysthyroïdie) étaient les plus documentés car considérés comme ayant des conséquences graves (impact personnel familial, professionnel et/ou social).
Les cas ont été analysés selon deux approches :
- une approche globale par l’analyse du nombre de cas et la description des effets indésirables (EI) par classe organe (selon le dictionnaire MedDRA), pour identifier d’éventuels effets inattendus (de par leur nature, leur gravité ou leur fréquence) ;
- une approche approfondie au cas par cas des observations de la BNPV évoquant une dysthyroïdie, permettant d’identifier les observations pour lesquelles la chronologie de prise de LEVOTHYROXnouvelle formule et des valeurs de TSH sont documentées.
Cinq effets indésirables en moyenne par cas (signalement)
Parmi les 5 062 cas les plus documentés de la BNPV, 25 151 effets indésirables ont été notifiés, chacun de ces patients signalant donc en moyenne 5 effets indésirables.
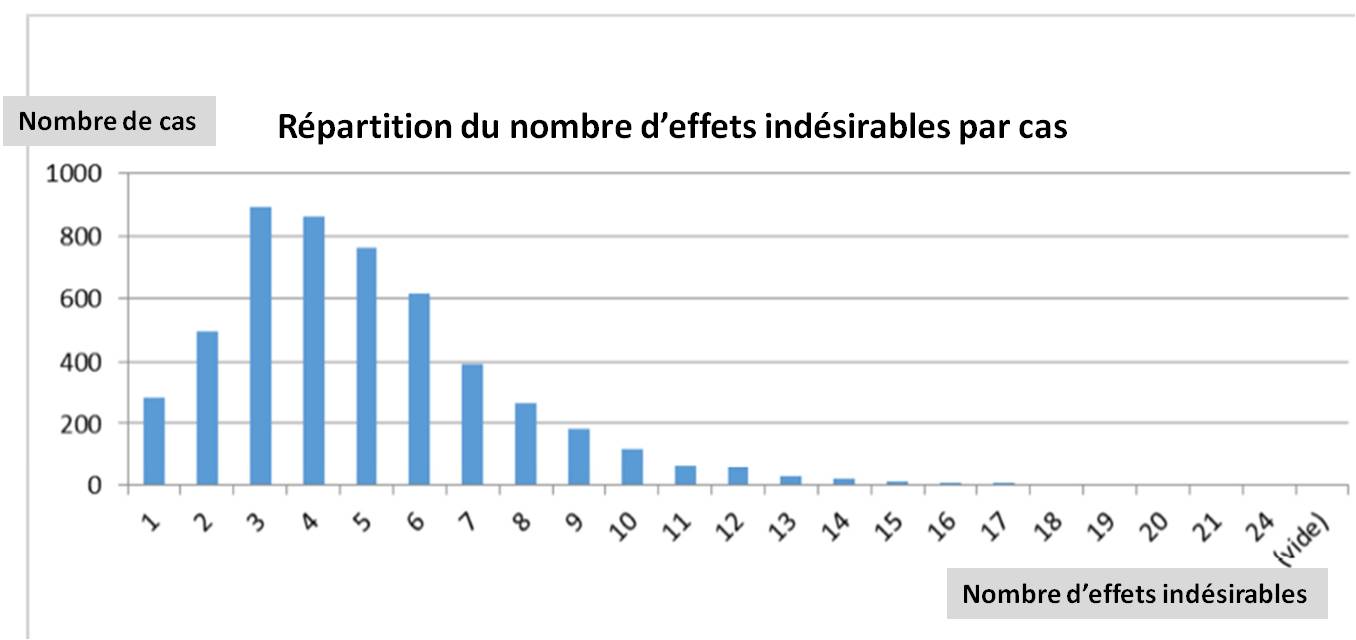
Parmi les patients déclarant un ou plusieurs effets indésirables, plus de 90 % sont des femmes
Cette analyse a apporté des précisions sur les caractéristiques démographiques de la population déclarante.
Elle est représentée majoritairement par des femmes (90,7 % de femmes et 9,3 % d’hommes) et l’âge moyen des déclarants est de 53,4 ans +/- 13,7 ans.
L’ANSM rappelle qu’en France, l’incidence annuelle de l’hypothyroïdie avérée est estimée à 4/1000 chez les femmes et inférieure à 1/1000 chez les hommes (SFE-HAS 2007). La revue Prescrire cite les chiffres de 0,1 à 2% des adultes qui présenteraient une hypothyroïdie avérée, précisant que cette pathologie est 5 à 8 fois plus fréquente chez les femmes que chez les hommes (Rev Prescrire 2015).
Des effets indésirables non spécifiques mais bien plus fréquents depuis juillet (avant la crise médiatique d’août – septembre)
Les EI les plus fréquemment rapportés étaient :
- de la fatigue,
- des maux de tête,
- de l’insomnie,
- des vertiges,
- des douleurs articulaires (arthralgies) et/ou musculaires (myalgies),
- une chute de cheveux (alopécie)
Par contre, les auteurs de l’ANSM ont constaté une forte hausse des signalements après mars 2017, en particulier en juillet (avant le début de la crise médiatique et sur les réseaux sociaux) et en août, comme vous pouvez le visualiser sur ce grapique réalisé à partir des données du tableau 1 page 16 du rapport de l’enquête de pharmacovigilance de l’ANSM :
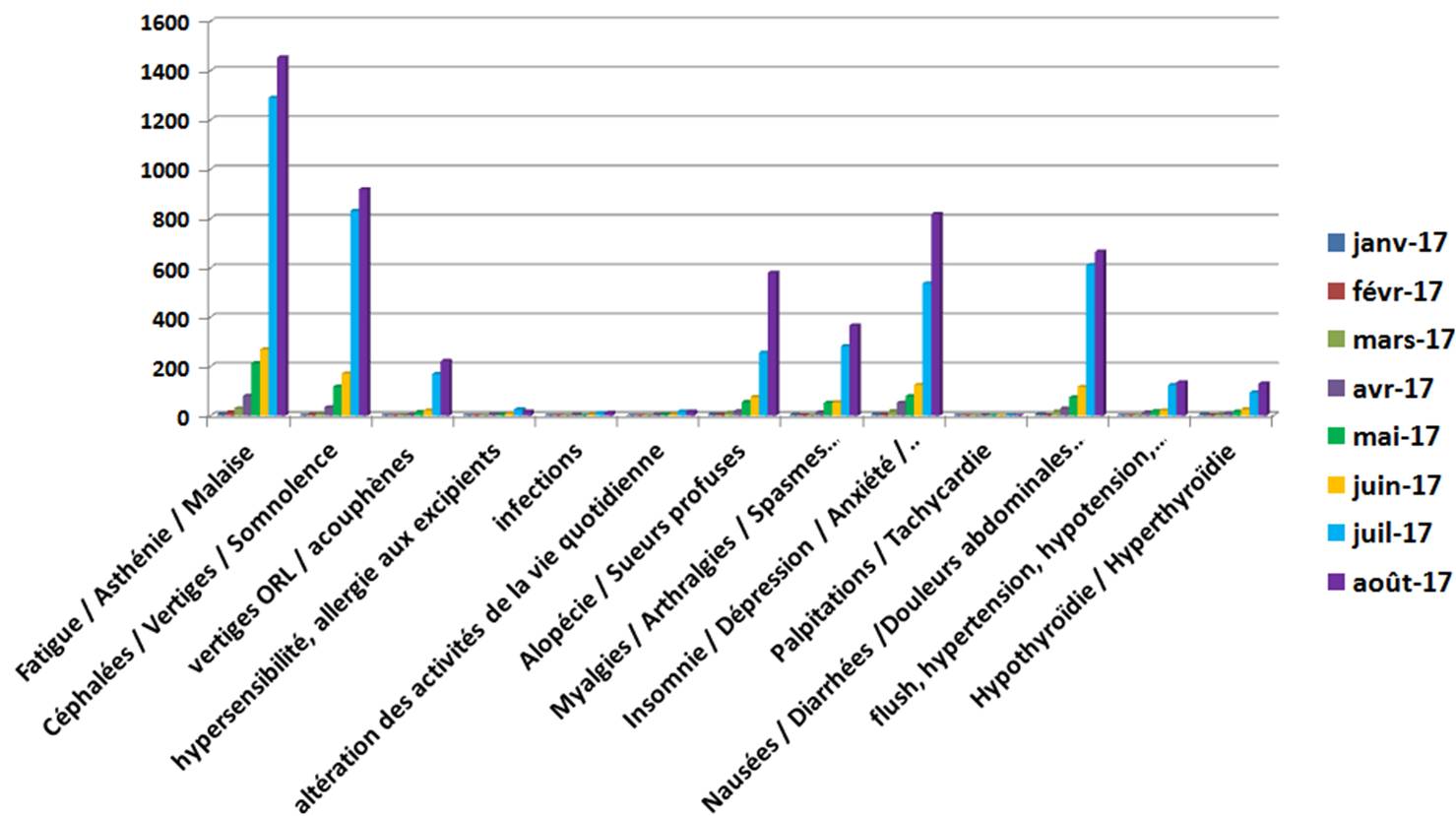
Le constat de cette hausse survenue surtout en juillet et en août est probablement lié à la demi-vie longue de la levothyroxine, retardant l’apparition d’éventuels déséquilibres thyroïdiens.
Analyse au cas par cas : des situations de dysthyroïdie attendues…
L’analyse détaillée des cas de la BNPV de déséquilibres thyroïdiens avec une TSH documentée avant et après passage à LEVOTHYROX NF (396 observations sur 1150) a permis d’identifier 178 cas d’hypo ou d’hyperthyroidie confirmés par des valeurs de TSH en dehors des normes attendues(7 avant mars 2017, cf. graphe ci-dessus, tout à droite).
Ces effets étaient attendus et avaient d’ailleurs motivé l’ouverture de l’enquête en mars 2017. Ils concernent a priori des patients davantage sensibles à de très faibles variations de doses de lévothyroxine, sans facteurs prédictifs.
Mais une symptomatologie non spécifique observée chez certains patients, sans lien apparent avec une dysthyroïdie. D’autres facteurs en cause ?
Cette analyse individuelle permet également de mettre en évidence une symptomatologie aspécifique, associant des signes d’hypo- et d’hyperthyroïdie, alors que le taux de TSH est normal.
La présence de signes cliniques chez ces patients à TSH dans les normes attendues suggère que des facteurs autres qu’une dysthyroïdie interviennent, sans plus de précisions.
Pour les auteurs de l’enquête, cette observation mérite plus d’investigations.
Les vertiges, nouveaux symptômes ou non ?
Les auteurs notent que les vertiges ne rentrent pas dans un tableau d’hypothyroïdie ou d’hyperthyroïdie.
Is sont pourtant retrouvés dans les effets indésirables rapportés avec la nouvelle formule, mais aussi avec l’ancienne formule, certes en nombre inférieur (mais comme pour d’autres effets indésirables). Il ne s’agit donc pas d’un nouvel effet indésirable.
Un ajustement des doses qui semble moins efficace qu’un retour à l’ancienne formule…
Les deux tiers des patients présentant une hyperthyroïdie ont eu un ajustement des doses.
Les auteurs ont constaté que les effets indésirables chez les patients ayant eu un tel ajustement restent identiques à ceux des patients non rétablis, à savoir fatigue/asthénie, variation de la TSH, céphalées, vertiges, palpitations, insomnie, poids augmenté, contractures musculaires/myalgies.
Dans les signalements où les patients reviennent à l’ancienne formule (EUTHYROX) ou switchent vers une alternative, « les symptômes régressent en général dans un délai très court », résume l’ANSM.
…mais il est possible que cette absence d’efficacité soit liée au manque de recul
Le fait que 33 % des patients en hyperthyroïdie n’aient eu aucun ajustement de posologie « peut en partie expliquer la persistance des symptômes,voire l’apparition d’autres symptômes », selon l’ANSM.
Pour l’ANSM toujours, « l’absence d’évolution favorable des signes cliniques après une modification de dose chez des patients à TSH en dehors des valeurs normales est difficilement interprétable car le recul sur l’impact de l’ajustement de la dose est souvent insuffisant pour conclure (délai entre modification de posologie et signalement inférieur à 1 mois) ».
En conclusion : des premiers éléments de compréhension mais des inconnues nécessitant des travaux complémentaires
Ces résultats intermédiaires montrent la fréquence élevée de signalements suite à la mise à disposition de la nouvelle formulation de LEVOTHYROX, ce qui justifie a posteriori l’inquiétude massive manifestée sur les réseaux sociaux : les signalements sont montés en flèche dès juillet, cf; graphique ci-dessus et illustrant cet article.
Cependant, l’ANSM estime qu’aucun nouveau signal de pharmacovigilance, marqué par des effets indésirables de nature ou de gravité spécifique à la nouvelle formulation, n’a été identifié.
Des investigations complémentaires sont cependant nécessaires pour comprendre l’apparition de signes d’hypo ou d’hyperthyroïdie malgré des dosages de TSH dans les normes attendues.Est-ce dû à des facteurs non identifiés ?
L’enquête de pharmacovigilance se poursuit et devra, au cours des prochaines semaines, prendre en compte l’arrivée des nouveaux médicaments à base de lévothyroxine (l-THYROXIN HENNING à partir du 16 octobre, puis un autre médicament en novembre). Elle devra aussi vérifier si l’ajustement des doses permet, ou pas, de corriger l’apparition de symptômes (avec du recul).
Après avoir pris connaissance de ces premières conclusions, le CTPV souhaite que soit mis en place un groupe de travail constitué de professionnels de santé, pharmacovigilants et patients afin de discuter de ces cas aspécifiques.
En parallèle, l’ANSM a lancé une étude de pharmacoépidémiologie pour étudier les effets du changement de formule sur l’ensemble des patients traités.
Pour aller plus loin
Point d’actualité sur le Levothyrox et les autres médicaments à base de lévothyroxine – Communiqué (ANSM, 11 octobre 2017)
Enquête de pharmacovigilance LEVOTHYROX (ANSM, 11 octobre 2017)
Sur VIDAL.fr
L-THYROXIN HENNING (lévothyroxine) : 4 dosages disponibles à partir du 16 octobre (12 octobre 2017)
Levothyroxine : aides à l’initiation et à la gestion des difficultés, nouvelles importations d’EUTHYROX (5 octobre 2017)
EUTHYROX (« ancien LEVOTHYROX ») en pharmacie le 2 octobre : conditions de prescription et délivrance (28 septembre 2017)
LEVOTHYROX : évaluation par 2 900 médecins de l’impact de la nouvelle formulation (enquête VIDAL) (28 septembre 2017)
Levothyroxine : retour temporaire de l’ancienne formule du LEVOTHYROX, nouvelles spécialités annoncées (15 septembre 2017)













